En este vídeo vamos a explicar las
soluciones a las preguntas
y cuestiones planteadas en la
práctica para la determinación
y cuantificación de inmunoglobulinas
en la saliva
mediante la técnica de Lisa.
En la explicación de la introducción,
si se decía que la inmunoglobulinas
es la mayoritaria en las secreciones
y existe una patología que
la deficiencia selectiva
igea que es un embudo,
difícil de primaria,
que se explicaba que era
la más frecuente,
esta es una de las preguntas que
se hacían en la práctica,
la mayoría de las personas afectadas.
Son asintomáticos estas
preguntas y bueno,
y algunos sí que son afectados,
que puede llegar
a haber consecuencias graves
en alguno de ellos,
y las infecciones más recurrentes
son el tracto digestivo respiratoria,
pues otra posible pregunta
en los cuestionarios
respecto a la técnica que se
comentó en la práctica,
que había varios tipos.
En concreto,
en esta se utilizaron un
tipo sandwich directo
y se va a venir Igea en
saliva en la técnica,
y esa es siempre un soporte
sólido que se puede unir,
o bien el antígeno del anticuerpo en
nuestro caso es el anticuerpo anti
inmunoglobulinas humana por
tanto la capa de captura
tenemos la inmunoglobulinas a
humana en la capa problema,
tenemos nuestras muestras de saliva
o bien las muestras, patrón,
y, en la capa de detección tenemos
el anticuerpo anti
inmunoglobulinas humana, unido al
enzima a la oxidación Vanesa
son selectivamente, aleatoriamente,
le habrá tocado algún estudiante
alguna de estas tres preguntas?
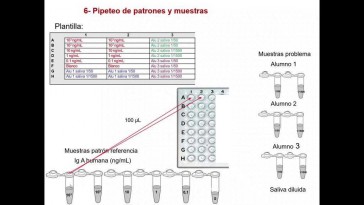
Este es el esquema resumido de
el protocolo de realización
de la práctica,
donde primero se se tapizan con
el anticuerpo de captura.
Esta sería la capa de captura
después de incubar toda la noche
y lavar se añade las muestras.
Este problema después de
encubrir elaborar,
se añadiría.
La capa de detección, es decir,
al anticuerpo con la después.
Y se produciría,
si apareciera un producto que
tiene color, las se mediría
y se representaría la concentración
respecto a la observancia,
pudiendo trazar una recta
de calibrado
y un rango de sensibilidad sobre
el cual podríamos extrapolar
los valores de observancia de
las muestras problemas
y dar un valor.
Una de las preguntas que os hacen es
cuál es la concentración del
anticuerpo de captura.
Algunos me habéis dicho 400.
Evidentemente 400 es el dial de
anticuerpo de captura que os damos,
pero no es el la concentración
que aparecen los pozos
y ahora tenéis que calcular cómo
ya pusimos en la introducción.
Se utiliza la fórmula de
concentración por volumen.
Concentración inicial en
la que estábamos.
El tubo es de 400 microgramos
mililitros
el volumen que tenéis que añadir;
es 38.000 litros;
y el volumen finales,
2.476 micrómetros,
solamente tienes que aplicar la
fórmula de la concentración
que sale es seis con 14 microgramos
mililitro que esa es la respuesta
a la pregunta.
A qué concentración de anticuerpos
se trabajan en el ensayo para
el anticuerpo de detección,
es decir, la capa de detección
os vuelven a os?
Preguntan en este caso
el volumen que estamos utilizando
entonces aplicando la fórmula;
igualmente el volumen final es dos
con seis la concentración
que queremos preparar, estilo
24.000 mililitros
y cómo el vial que proporcionaba
majestad acero,
ocho microgramos mililitros la
única incógnita que tenéis
que despejar es cuánto volumen
tienes que coger de este tubo
para preparar vuestra disolución y
la respuesta es 78 mililitros.
El volumen final está compuesto
por el volumen de tampón
y el volumen de anticuerpo;
por tanto, si dos con seis
el volumen final,
el volumen se desea que tenéis
que añadir; uno con 82,
añadirle 78 tener ya dos con seis
litros de la anticuerpo de detección
para preparar la mezcla, que
lleva sustrato y sustrato,
como la enzima, de la penosidad,
sustratos.
El peróxido de hidrógeno y homogéneo
es la 1, dos feliz
ni a Mina, que es el que tiene
color amarillo naranja
cuando se oxiden este
sustrato homogéneo;
viene en pastillas.
En comprimidos que pesan 20
miligramos mililitros
como ya explicamos en la
introducción, lo que nos pide;
la práctica es calcular o preparar
el cromosoma nacer o cinco miligramos
-mililitros y por tanto
necesitamos saber
qué volumen de disolvente tenemos
que añadir para prepararlo.
Se le sustituye la fórmula
-concentración más polvo,
uno menos y por tanto,
tenemos la respuesta al
volumen final total
que necesitamos para diluir ese
comprimido serían 40 mililitros;
si no hubiera otro susto; si no
hubiera otra molécula más,
se haría directamente, pero
necesitamos el sustrato
de la reacción, que es el
peróxido de hidrógeno.
Por tanto, en este volumen final
van a participar, el trato
que se diluye
y el volumen que va a ocupar el
peróxido de hidrógeno vale.
Esto está en polvo; tenemos que
tener en cuenta la masa,
pero el peróxido de hidrógeno ya
viene disuelto; diluida en agua
y, por tanto, tenemos un
valor de concentración
para calcular qué volumen
necesitamos,
pues aplicamos nuevamente la fórmula.
La concentración original
es tres por 100.
Volumen, volumen.
El volumen inicial es lo
que queremos saber.
Cuánto volumen tiene que coger de
hidrógeno para preparar un volumen
final de 40 ml que este dato lo
calculado a partir de la dos fines
de Amina y la concentración final
que me piden es cero puntos a 5,
porcentaje; volumen, monumento,
es un dato de concentración,
es una unidad de medida
de concentración.
Solo tenéis que sustituir
despejar la fórmula
y obtener que el volumen de peróxido
de la disolución de hidrógeno,
que necesitáis es como
a seis 7.000 litros.
Entonces, en el volumen final,
que son 40 mililitros
pero 6, 6, siete mililitros son
de la disolución de hidrógeno
por tanto restantes
y el volumen restante hasta 40.
Es decir, 39 contactos, 33
de volumen de trato,
en la práctica, si os dice
que los comprimidos,
no aportan volumen para que no
tienes que tener que tenerlo en cuenta.
Una vez que tenemos todo el
proceso experimental
realizado la reacción, se detiene
con ácido sulfúrico
y tenemos está en los pozos con este
color amarillo anaranjado
donde hay producto y se introduce
en el espectro fotómetro.
En este caso es un lector
de placa de lista
para que mida lapso a 400
no aumenta nanómetros
en cada uno de los.
Cuando el aparato mide.
Nos da 1.
Nos imprime podemos imprimir
un papel.
No nos salen en pantalla la lectura
de cada uno de ellos
solamente os represento la lectura
de los que tienen volumen.
El resto sería hacer.
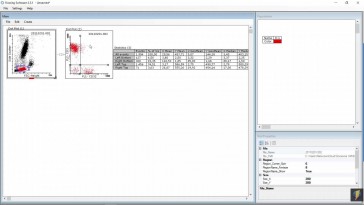
Entonces lo que tenemos que hacer
es con estos datos que aparecen
en la práctica no obtener ese anexo
uno el ejemplo de el resultado.
Que se obtendría de este ensayo
pues tenéis que localizar
e identificar el valor de de
cada uno de los pasillos.
Os acordáis?
Teníamos marcado en los grupos de 3.
La recta patrón está marcada
en rojo de los de la f
uno dos porque iban por
duplicado el alumno;
uno aparecen azul el dos en
verde y el tres en rosas
y que lo que hacemos es.
Marcarnos para saber a quién.
Corresponde cada uno de esos
valores; a continuación,
rellenamos la tabla que nos plantea
la práctica colocando,
identificando cada uno de los
valores con el pozo que corresponde.
Vale.
Pasamos los datos a la tabla
y ahora lo que hacemos
son los cálculos de las media neta
que necesitamos para poder hacer
la representación gráfica.
Entonces El Pozo y yo.
F 1.
F dos son los valores del blanco,
y para realizar los cálculos con
las organzas media neta
necesitamos saber las
media del blanco
y restarse al resto de ellos.
Así que se hace el cálculo.
Por tanto, el blanco.
La concentración cero de
inmunoglobulinas equivale
a la solvencia de cobro.
Entonces estos son los datos
con los que tenemos
que trabajar media neta con
los datos de la recta,
de la hemoglobina concentración
conocida.
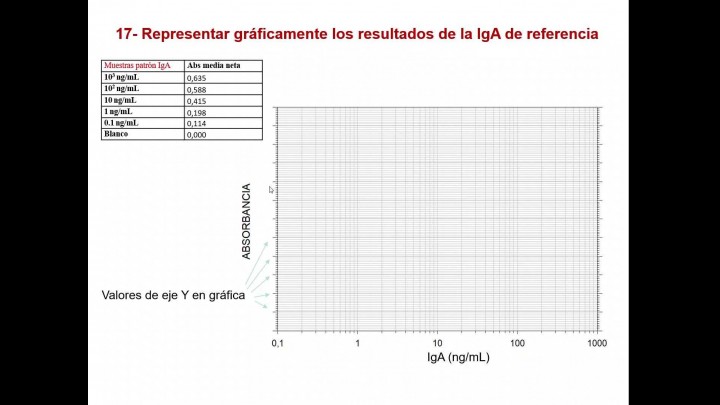
Se va a dibujar los datos
de la gráfica
y cuando se tengan entonces vamos a
llevar nuestros datos problema
para calcular a qué concentración
equivale a ese valor de entonces.
Cogemos los datos de
la muestra patrón,
los tenemos aquí las canciones
tenemos aquí nuestra gráfica.
Acordaron concentración y lineal
las como comentaban
-los valores de los.
Podéis dibujar en la escalada
siempre lineal,
pero la separación como queráis,
los que debéis hacerlo gráfica,
lo más ancha posible,
que no nos todos los datos
en la parte de abajo.
Entonces, uno de los un ejemplo
de cómo ha distribuido esto,
podía llegar a 1.
Cada uno puede hacer
con lo que quiera,
siempre y cuando se respeten los
valores y la genialidad.
Vale, en este caso yo aquí dibujado
que el máximo ser 8.
Por tanto, la mitad sería 0.
4, por tanto, a la mitad
serían cerdos.
Estos serían los valores
de estos puntos
y una vez que los tengo pues cálculo.
La distancia que hay entre
esta estrella este
y entonces poco los datos de lo
primero es poner mi escala,
determinar el máximo
y poner los datos,
bien puestos, haciendo los cálculos
bien para que la representación
sea correcta y después lo
que hacemos es proceder
a ir poniendo cada uno de los
datos sobre la gráfica.
Bien, pues empezamos
por el valor cero
nanogramos mililitros la solvencia
que tienen es de cero uno uno cuatro
vale pues buscamos el valor lo
pintamos vale este punto
es el valor de uno Tiene una
observancia de cero con 198,
pues aquí tenemos el 1, nos vamos
a hacer realmente y 8,
se dibuja en otro punto el de 10,
es decir, y el tenis.
Vale?
Pues ya tenemos cada
uno de los puntos
y unimos un trazo sobre cada
uno de esos puntos
y obtenemos una curva,
se donde hay al principio de la
concentración no es suficiente
para que sea proporcional.
Llega un momento que la
cantidad de Igea
empieza a tener un producto de color
que empieza a ser proporcional.
Hay una parte lineal
en donde conforme se aumenta la
concentración, aumenta el color,
el producto, las organzas y llega
un momento que se satura.
Ya no hay más encima
y, por más que añadamos sustrato,
no va a haber más producto,
vale?
En esta parte, la línea
ya está saturada
y hace como una muy bueno pues ya
tenemos nuestra gráfica dibujada.
Ahora necesitamos una vez que hemos
visto cuál es la parte lineal,
hacer la recta trazar la
recta de calibrado
y determinar los límites de
sensibilidad de nuestro ensayo.
Bien, pues esto es la zona
lineal y, por tanto,
ajustamos una recta a
los tres puntos,
en este caso que los he dibujado,
un poco que separaba la recta.
En este caso no hay encima
ninguno de los tres
pero deja aproximadamente
izquierda a derecha.
La misma distancia ésta sería
nuestra recta de calibrado,
y la rango de detención de este
ensayo sería los valores,
dentro de los cuales somos capaces
de dar un valor de concentración
con exactitud, es decir,
que en el rango entre dos
seis todos los valores
de entren en este rango van
a caer en la zona lineal
y, por tanto, para esa vamos a poder
dar un valor de concentración
esa es mi rango de sensibilidad
y yo puedo medir
de uno hacienda mililitros y
el rango de sensibilidad;
observancia sería desde
cero 98 acero, con 5,
8, ocho por encima de ese valor
o por debajo de ese valor
no podemos dar un dato
de concentración
con esa actitud vale,
podríamos decir que es menor que
mi rango de sensibilidad.
Si es por debajo de 0, dos menor
de un nanogramos mililitros
y si está por encima los valores que
estén por encima de su hermano,
de 5, 8, ocho no podemos dar
el dato con esta actitud,
pero podemos decir que son mayores
de el límite superior, que es bueno.
Una vez que tenemos nuestra
gráfica dibujada,
la recta de calibrado, calculada
y los rangos de sensibilidad
del ensayo determinados.
Pasamos a calcular la concentración
de nuestra muestra,
la tabla.
Tenemos los valores de neta
de cada uno de los y lo que
hacemos es dibujarlo;
en primer lugar, alumno, uno
saliva a una dilución
unos 50 es cero con cinco uno
tres ocho buscamos el valor
en la gráfica y extrapolar,
los llevamos a la a dónde corta
la recta de calibrado,
y vemos en qué punto corta.
En el eje de las equis,
un error frecuente
como sabéis, esto es,
si esto es bueno,
yo estoy 10.
El siguiente número es el 2, 3, 4,
si estos 10 estos tienen.
El siguiente número es 20, 30, 40.
Por tanto, el punto de
corte en el eje
para el primer para nuestra primera
muestra sería, pues entre 30 40,
los 38 nanogramos mililitro
el alumno 1,
la muestra que está diluida a 1.500.
El valor de fiestero con cero 4, 1,
8, por tanto está por debajo,
estaría por debajo del rango
de sensibilidad.
No podemos dar un dato exacto, pero
podemos decir que es menor
de nuestro límite inferior
es un menor para el 1,
dos haríamos lo mismo a una
concentración, unos 50,
se sale de nuestro rango
de función detección.
Por tanto podemos decir que es
mayor de 100 mililitros
pero no podemos dar su
valor con exactitud
cuándo vamos a las dilución 1.500,
si entran rango cero 5,
vemos en qué punto corta la recta
y calculamos la concentración,
que es aproximadamente veintiseis
nanogramos por litro.
Para el 1, tres ocurre lo mismo,
está saturado, el uno 50 se sale de
escala por la parte de arriba,
con lo cual mayor de 100 mililitros
y para la 50 a vamos hasta
la recta de calibrado.
Y vemos a qué datos de concentración
corresponde el número
y que se corta.
El eje es aproximadamente tres
con ocho nanogramos
mililitros bien,
pues ya tenemos los valores de
concentración en los pasillos,
y lo que tenemos que hacer ahora
es calcular la concentración en
la saliva del estudiante,
vale no en el pozo y yo sino
en la saliva original.
Si se acordar es para preparar
esta dilución es.
Partimos de la saliva original,
hicimos una dilución, unos 51.500.
Vale para para calcular
esa concentración
tengo que tener en cuenta
el factor de dilución.
Entonces en el uno 1,
el de unos 50 tiene 38.000
nanogramos mililitro.
Por tanto,
en la saliva de es estudiante
tenemos ese valor que aparece,
en el multiplicado por el factor
de dilución que hicimos valer.
En este caso de aquí aquí
tuvimos 50 veces.
Si yo tengo el dato de concentración,
aquí se multiplica por 50 para
saber la concentración.
En este caso sería.
1900.
Nanogramos por litro en
la tabla que os dan.
Os piden la concentración
en microgramos.
Mililitro único que tienes que hacer
es convertir las unidades 1900.
Nanogramos mililitros son uno
con nueve microgramos
-mililitros para el estudiante
2, la saliva del alumno; 2,
tenemos la dilución,
1.500; tenemos veintiseis nanogramos
1.000 litros, por tanto,
en la muestra original tendremos
veintiseis 1.539 1.000 nanogramos
mililitros por tanto 39 microgramos
por mililitro;
en el alumno; tres se hace
la misma operación
y el resultado son 5.700 nanogramos
mililitros que son
cinco con siete microgramos
mililitros en el caso
de la dilución, es 1.500 del alumno;
uno en ese es menor de un y la
saliva es menor que ese valor
multiplicado por 1.500 vale,
sería menos de 1.500.
En el alumno; dos sería mayor de
5.000 sería mayor de 5.000.
Hay otras cuestiones que puede
que os haya tocado
o no en relación a Al -al que
hayáis hecho preguntas
que se pueden hacer como que ocurre
cuando los volúmenes de anticuerpo
y captura son diferentes.
Cuáles serían los resultados
previstos?
Qué ocurre si no se hace
el primer lavado,
si nos hace el segundo lavado o si
no se hace el tercer lavado,
cuáles serían los resultados o qué
ocurre si hay diferencias
en el volumen de las muestras o en
el volumen de la de del patrón
o bien de sustrato para todas
esas posibilidades,
que además son a veces errores
reales de la práctica experimental
tenéis que os puede preguntar.
Cuáles serían las consecuencias
cuando tenéis los valores
de observancia,
y a veces hay cosas que no cuadran?
Pues tienes que saber dónde
ha estado el fallo,
en que pasó.
Os podéis haber equivocado y cuáles
serían las consecuencias?
De acuerdo?
Bueno, con esto terminamos, damos
por resuelta la práctica
y lo mismo cualquier duda
a mi correo María,
me punta.

![]() o pulsar la combinación de teclas Ctrl+V.
o pulsar la combinación de teclas Ctrl+V.